La enfermedad renal crónica afecta a más de 697 millones de personas en todo el mundo. En total, se estima que cada año mueren 1.2 millones de personas debido a esta enfermedad, lo que representa casi el 5% de todas las muertes anuales a nivel mundial. A pesar de la enorme carga económica y personal que esto conlleva, hasta ahora se desconocían cuáles eran los mecanismos biológicos detrás de esta afección, debido a la complejidad estructural y funcional del riñón.
En un estudio publicado en la prestigiosa revista Cell Metabolism, investigadores del Instituto de Bioingeniería de Cataluña (IBEC) y del CIBER-BBN, liderados por Núria Montserrat, en colaboración con investigadores de la Universidad de Pensilvania y del Instituto de Ciencia y Tecnología de Gwangju, han identificado los genes responsables de la enfermedad renal crónica y han demostrado que es posible revertir esta deficiencia, abriendo así una posible ruta terapéutica contra el daño renal.
Haciendo uso de técnicas innovadoras como la secuenciación de ARN a nivel de célula individual, los investigadores descifraron el papel crucial que desempeñan los genes del metabolismo lipídico a la hora de proteger frente a la insuficiencia renal crónica. Para ello, los análisis se realizaron con modelos animales y con minirriñones humanos, donde los resultados se validaron utilizando casi un centenar de muestras de pacientes.
En adultos sanos, cada uno de los nuestros riñones contiene un promedio de 1.5 millones de nefronas, las unidades funcionales básicas del riñón que filtran constantemente los productos de desecho de la sangre. Entre las diferentes células que conforman estas unidades de filtración, las células epiteliales del túbulo proximal de la nefrona son las encargadas de realizar la reabsorción de agua y solutos, representando el 90% del total de la masa renal. En casi todos los casos de enfermedad renal crónica, se produce un daño en estas células, pero hasta ahora, no se sabía qué mecanismos celulares eran los responsables de tal disfunción.
Mediante la secuenciación del ARN de cada una de las miles de células presentes en el riñón, los investigadores observaron por primera vez, diferencias importantes entre las células sanas y enfermas del túbulo proximal. En concreto, en los riñones de ratones con enfermedad renal crónica, detectaron que una mayor proporción de las células del túbulo proximal presentaban una firma molecular distinta a la encontrada en los riñones de animales sanos.
Ante estas observaciones, las investigadoras de IBEC dieron un paso más y, utilizando minirriñones humanos, demostraron que estos cambios eran debidos a una disminución en la expresión de algunos de los genes que regulan el metabolismo de los lípidos en las células del túbulo proximal. Además, "gracias a un abordaje multidisciplinar, utilizando modelos animales y minirriñones humanos que generamos mediante bioingeniería en el IBEC descubrimos que, al corregir esta deficiencia, las células del túbulo proximal podían recuperar su función en los diferentes modelos de estudio", explica la Dra. Montserrat.
Combinando la secuenciación de ARN a nivel de célula individual, y el uso de bioingeniería para producir minirriñones, fue posible identificar a nivel celular las diferencias clave entre los riñones sanos y enfermos.
Los minirriñones humanos —también denominados organoides de riñón— están creados mediante técnicas de bioingeniería a partir de células madre humanas, y recogen algunos aspectos de la complejidad de este órgano real. El pasado mes de abril, ya demostraron su eficacia como modelo de estudio al utilizarlos para descifrar en tiempo récord cómo el SARS-Co-V2 interacciona e infecta las células de estos minirriñones, además de identificar una terapia dirigida a reducir la carga viral.
En este estudio la secuenciación de ARN a nivel de célula individual de las muestras de los minirriñones se ha realizado en el laboratorio del Dr. Felipe Prósper, del CIBERONC, la Clínica Universidad de Navarra y CIMA Universidad de Navarra. “El riñón tiene más de 23 tipos de células diferentes”, explica la Dr. Montserrat. “Hace unos años, era necesario examinar múltiples muestras por separado para obtener la información, lo que podía llevar años de trabajo, ahora esta misma información la podemos obtener en pocos días”, y añade: “con la secuenciación de ARN de cada una de las células del riñón y utilizando múltiples muestras, podemos identificar qué genes están diferencialmente expresados en cada una de las células".
Estudiando estas diferencias o, dicho de otra manera, analizando la “firma” de la expresión del ARN de cada una de estas células, los investigadores identificaron que la disfunción del túbulo proximal es consecuencia de la desregulación de una vía metabólica clave. Específicamente, en las muestras enfermas de ratones, también se halló una mayor proporción de células inmaduras. “Se sabe que una pequeña proporción de las células de los túbulos proximales del riñón presentan un comportamiento similar al de las células madre”, señala Carmen Hurtado del Pozo, investigadora del IBEC y coautora del estudio. “Cuando se producen daños en el riñón, el túbulo proximal tiende a responder muy rápidamente ya que puede restaurar las partes de la nefrona que están lesionadas. Sin embargo, durante la enfermedad renal crónica, estas células pierden su capacidad regenerativa", suscribe la Dra. Montserrat.
Este trabajo ha identificado los genes metabólicos que se desactivan cuando el riñón está sometido a un daño crónico, perdiéndose la “firma” sana en las células del túbulo proximal del riñón. Para esa firma, el receptor de estrógeno alfa (ESRRa, por sus siglas en inglés) es uno de los marcadores que tiene un papel más relevante. “Estos genes son especialmente importantes para las células del túbulo proximal, ya que necesitan tener un metabolismo muy activo. De hecho, después de las células del corazón, son estas células, las que tienen el mayor requerimiento energético de nuestro cuerpo”, explica la Dr. Montserrat. "Cuando la expresión de los genes que controlan el metabolismo de los lípidos disminuye, el riñón pierde su capacidad de responder frente al daño", añade la Dra. Hurtado del Pozo.
Mediante la generación de minirriñones, las investigadoras pudieron simular condiciones de cultivo con el fin de manipular los niveles de ESRRa en las células de estos miniórganos. Cuando se volvió a encender el ESRRa, el túbulo proximal parecía volver a recuperar su función. Tales observaciones se daban en los modelos animales que los colaboradores de la Universidad de Pensilvania —quienes hace dos años ya publicaron, por primera vez, el uso de la secuenciación de ARN a nivel de célula individual en riñones de ratones sanos.
Este trabajo demuestra que la combinación de tecnologías emergentes, como la secuenciación de ARN a nivel de célula única y los miniórganos, pueden ser muy ventajosas a la hora avanzar en investigación biomédica. Este estudio propone que junto a ESRRa existen otros receptores nucleares que pueden actuar, en un futuro cercano, como dianas terapéuticas para revertir la enfermedad renal crónica.
El estudio ha estado codirigido por la investigadora del CIBER-BBN Nuria Montserrat, Profesora de Investigación ICREA e Investigadora principal del grupo “Pluripotencia para la regeneración de órganos” del Instituto de Bioingeniería de Cataluña (IBEC), el Dr Katalin Susztak de la Universidad de Pensilvania y el Dr Jihwan Park del Instituto de Ciencia y Tecnología de Gwangju.
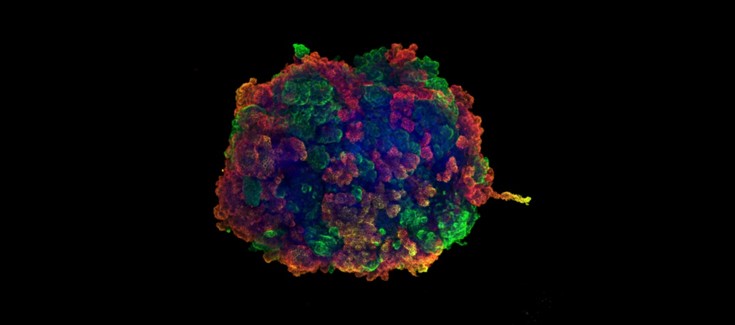
Imagen: microscopía confocal de un organoide de riñón generado in vitro a partir de células madre pluripotentes humanas que han sido diferenciadas durante 20 días usando cultivos tridimendionales. Estos organoides de riñón contienen estructuras renales que incluyen túbulos proximales (marcados con LTL, en verde) y podocitos (que expresan PODXL, en rojo) que se asemejan en parte a las estructuras renales del riñón humano.
The Nuclear Receptor ESRRA Protects from Kidney Disease by Coupling Metabolism and Differentiation https://www.cell.com/cell-metabolism/fulltext/S1550-4131(20)30606-9o